Experimental Studies to Optimize Process Parameters for the Removal of Cationic and Anionic Dyes by Natural Cypress Leaves
DOI:
https://doi.org/10.29356/jmcs.v68i3.2037Keywords:
Brilliant green, lanasyn black, cypress leaves, adsorption, Taguchi methodAbstract
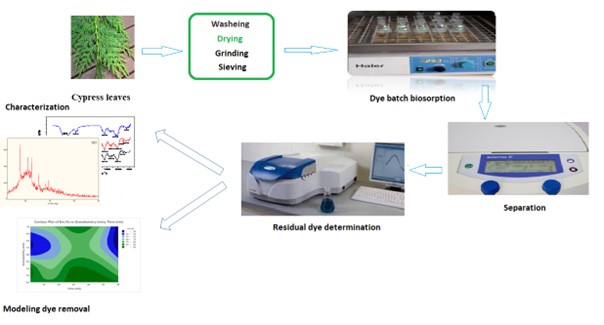
Abstract. In this study, cypress leaves were used for the preparation of a biosorbent to remove brilliant green (BG) and black lanasyn (LB) from aqueous solutions. The influence of several experimental factors, such as time of contact, pH, initial concentration, ionic strength, temperature, stirring speed, and particle size, on the adsorption of these dyes was studied. Contact time s'effect has showed that balance was reached at 30 min with adsorption capacities 9.24 and 4.08 mg/g and elimination rates of 95.97 % and 34 % for BG and LB, respectively. Moreover, the study has shown that the adsorption of the two dyes can be described by pseudo-second-order kinetics. The adsorption isotherms demonstrated that the Freundlich model was satisfactory compared with the Langmuir model for describing the process of adsorption of the two dyes on the cypress. The results showed that the adsorption process is spontaneous, feasible, and endothermic for BG and non-spontaneous and exothermic for LB. Multi-docking reflecting the biosorption of brilliant green and Lanasyn black on the adsorbant surface is proposed. On the fundamental plane, the fractional orthogonal Taguchi plane L16 (45) was used to optimize the conditions for brilliant green adsorption on the cypress. In conclusion, the results showed that cypress leaves could be advantageously used as a low-cost biosorbent for the removal of brilliant green and lanasyn black in wastewater treatment.
Resumen. En este estudio se usaron hojas de ciprés para preparar un biosorbente que remueve los colorantes verde brillante (BG) y lanasyn negro (LB) de soluciones acuosas. En la adsorción de estos colorantes se estudió la influencia de varios factores experimentales como tiempo de contacto, pH, concentración inicial, fuerza iónica, temperatura, velocidad de agitación y tamaño de partícula. El efecto del tiempo de contacto mostró que el balance se alcanzó a los 30 min con capacidades de adsorción de 9.24 y 4.08 mg/g y velocidades de eliminación de 95.97 % y 34 % para BG y LB, respectivamente. El estudio mostró que la adsorción de los dos colorantes se puede describir por una cinética de pseudo segundo orden. Para describir el proceso de adsorción de los dos colorantes en las hojas de ciprés, las isotermas de adsorción demostraron que el modelo de Freundlich es satisfactorio comparado con el modelo de Langmuir. Los resultados muestran que el proceso de adsorción es espontáneo, factible y endotérmico para BG, y no espontáneo y exotérmico para LB. Se propone un acoplamiento múltiple reflejando la biosorción del verde brillante y el lanasyn negro sobre la superficie del adsorbente. En el aspecto fundamental, la fracción ortogonal del plano de Taguchi L16 (45) se utilizó para optimizar las condiciones de adsorción del verde brillante en las hojas de ciprés. En conclusión, los resultados muestran que las hojas de ciprés pueden utilizarse como biosorbentes de bajo costo para la remoción de verde brillante y lanasyn negro en el tratamiento de aguas residuales.
Downloads
References
Li, X.; Li, J.; Shi, W.; Bao, J.; Yang, X. Mater. 2020, 13, 332. DOI: https://doi/10.3390/ma13020332. DOI: https://doi.org/10.3390/ma13020332
Aksu, Z.; Tezer, S. Process. Bio. chem. 2005, 40, 1347–1361. https://doi/10.1016/j.procbio.2004.06.007. DOI: https://doi.org/10.1016/j.procbio.2004.06.007
Forgacsa, E.; Cserhatia, T.; Oros, G. Environ. Int. 2004, 30, 953–971. DOI: https://doi/10.1016/j.envint.2004.02.001. DOI: https://doi.org/10.1016/j.envint.2004.02.001
Bhattacharya, K. G.; Sharma, A. Dyes. Pigm. 2005, 65, 51–59. DOI: https://doi/10.1016/j.dyepig.2004.06.016.
Fernandez, M. E.; Nunell, G. V.; Bonelli, P.R.; Cukierman, A. L. Bioresour. Technol. 2010, 101, 9500–9507. DOI: https://doi/10.1016/j.biortech.2010.07.102. DOI: https://doi.org/10.1016/j.biortech.2010.07.102
Kismir, Y.; Aroguz, A. Z. J. Chem. Eng. 2011, 172, 199–206. DOI: https://doi/10.1016/j.cej.2011.05.090. DOI: https://doi.org/10.1016/j.cej.2011.05.090
Belov, S.; Naumchik, G. E3S. Web. Conf. 2020, 212, 1-10. DOI: https://doi/10.1051/e3sconf/202021201001.
Papic, S.; Koprivanac, N.; Bozic, A. L. C. Color. Technol. 2000, 116, 352-358. DOI: https://doi/10.1111/j.1478-4408.2000.tb00013. DOI: https://doi.org/10.1111/j.1478-4408.2000.tb00013.x
Adosinda, M.; Martins, M.; Nelson, L.; Silvestre, A. J. D.; Queiroz, M. J. Chemosphere. 2003, 52, 967–973. DOI: https://doi/10.1016/S0045-6535(03)00286-8. DOI: https://doi.org/10.1016/S0045-6535(03)00286-8
López, C.; Valade, A. G.; Combourieu, B.; Mielgo, I.; Bouchon, B.; Lema, J. M. Anal. Biochem. 2004, 335, 135–149. DOI: https://doi/10.1016/j.ab.2004.08.037. DOI: https://doi.org/10.1016/j.ab.2004.08.037
Calabro, V.; Pantano, G.; Kang, R.; Molinari, R.; Drioli, E. Desalination. 1990,78, 257-277. DOI: https://doi/10.1016/0011-9164(90)80046-E. DOI: https://doi.org/10.1016/0011-9164(90)80046-E
Van Der Bruggen, B.; Lejon, L.; Vandecasteele, C. Environ. Sci. Techn. 2003, 37, 3733-3738. DOI: https://doi/10.1021/es0201754. DOI: https://doi.org/10.1021/es0201754
Anselme, C.; Jacobs, E. P. Water treatment membrane processes, New York. McGraw Hill Mallevialle. 1996, 401-1087.
Andreozzi, R.; Caprio, V.; Insola, A.; Marotta, R. Catal. Today. 1999, 53, 51-59. DOI: https://doi/10.1016/S0920-5861(99)00102-9. DOI: https://doi.org/10.1016/S0920-5861(99)00102-9
Koch, M.; Yediler, A.; Lienert, D.; Insel, G.; Kettrup, A. Chemosphere. 2002, 46, 109-113. DOI: https://doi/10.1016/S0045-6535(01)00102-3. DOI: https://doi.org/10.1016/S0045-6535(01)00102-3
Leszczyĕska, M.; Hubicki, Z. Desalin. Water. Treat. 2009, 2, 160–165. DOI: https://doi/10.5004/dwt.2009.254.
Brillas, E.; Mur, E.; Sauleda, R.; Sanchez, L.; Peral, J.; Domenech, X.; Casado, J. Appl. Catal. B: Environ. 1998, 16, 31-42. DOI: https://doi/10.1016/S0926-3373(97)00059-3. DOI: https://doi.org/10.1016/S0926-3373(97)00059-3
Oturan, M. A. J Appl Electrochem. 2000, 30, 477-478. DOI: https://doi/10.1023/A:1003994428571.
Boye, B.; Dieng, M. M.; Brillas, E. Environ. Sci. Technol. 2002, 36, 3030-3035. DOI: https://doi/10.1021/es0103391. DOI: https://doi.org/10.1021/es0103391
Bellakhal, N.; Dachraoui, M.; Oturan, N.; Oturan, M. A. J. Soc. Chim. Tun. 2006, 8, 223-228.
Lambert, S. D.; Graham, N. J. D.; Sollars, C. J.; Fowler, G. D. Water. Sci. Technol. 1997, 36, 173-180. DOI: https://doi/10.1016/S0273-1223(97)00385-5. DOI: https://doi.org/10.2166/wst.1997.0512
Lin, S. H. J. Chem. Technol. Biotechnol. 1993, 57, 387-391. DOI: https://doi/10.1002/jctb.280570415.
Ramakrishna, K. R.; Viraraghavan, T. Water. Sci. Technol. 1997, 36, 189-196. DOI: https://doi/10.1016/S0273-1223(97)00387-9. DOI: https://doi.org/10.2166/wst.1997.0516
Benamraoui, F. Master's thesis, Ferhat Abbas-Setif University, 2014, Algeria.
Khalifah, A.; Hayfaa, A. M.; Amoako, J.; Laith, A. A.; Al Khaddar, R.; Mawada, A.; Al-Janabi, A.; Hashim, K. S. Conf. Ser: Mater. Sci. Eng. 2020, 888, 012036. DOI: https://doi/10.1088/1757-899X/888/1/012036. DOI: https://doi.org/10.1088/1757-899X/888/1/012036
Gul, S.; Azra, G.; Hajera, G.; Rozina, K.; Muhammad, I.; Khan, S.U.; Khan, M. S.; Aouissi, H. A.; Andrejs, Krauklis. Mater. 2023, 2, 1-15. DOI: https://doi.org/10.3390/ma16020521.
Baidya, K. S.; Upendra, K. S. Afr. J. Chem. Eng. 2021, 35, 33-43. DOI: https://doi.org/10.1016/j.sajce.2020.11.001.
Samiyammal, P.; Kokila, A.L.A.; Rajakrishnan, R.; Rengasamy, S.; Ragupathy, S.M. K.; Vasudeva, R.M.R. Environ. Res. 2022, 212, 113497. DOI : https://doi.org/10.1016/j.envres.2022.113497.
Venkat, S.; Mane, P.V.; Vijay, B. Desalination. 2011, 273, 321-329. DOI: https://doi.org/10.1016/j.desal.2011.01.049.
Rehman, M. S.U.; Muhammad, M.; Muhammad, A.; Naim, R.; Muhammad, F.N.; Danish, M.; Han. J. Chem. Eng. 2013, 228, 54-62. DOI: https://doi.org/10.1016/j.cej.2013.04.094.
Nandi, B. K.; Amit, G.; Mihir, K, P. J. Hazard. Mater. 2009, 161, 387-395. DOI: https://doi.org/10.1016/j.jhazmat.2008.03.110.
Copaciu, F.; Virginia, C.; Mihaela, V.; Ocsana, O. JPC-J. PLANAR. CHROMAT. 2012, 6, 509-515. DOI: https://doi.org/10.1556/jpc.25.2012.6.4.
Amara-Rekkab, A. Int. J. Health. Sci. 2023, 7, 165–175. DOI: https://doi.org/10.53730/ijhs.v7n3.14657.
Belov, S.; Grigoriy, N. E3S. Web. Conf. 2020, 212, 01001. DOI: https://doi.org/10.1051/e3sconf/202021201001.
Samira, S.; DOMA, N. H. Sci. Total. Environ. 1989, 79, 71-279. DOI: https://doi/10.1016/0048-9697(89)90342-2.
Amara-Rekkab, A.; Didi, M.A. Desalin. Water. Treat. 2023, 28, 186–195. DOI: https://doi/10.5004/dwt.2023.29147. DOI: https://doi.org/10.5004/dwt.2023.29147
Amara-Rekkab, A.; Didi, M.A. J. Mater. Environ. Sci. 2021, 12, 603-615.
Omri, A.; Benzima, M. Desalin. Water. Treat. 2012, 51, 2317- 2326. DOI: https://doi/10.1080/19443994.2012.734585. DOI: https://doi.org/10.1080/19443994.2012.734585
Chandarana, H.; Ponnusamy, S. K.; Muthulingam, S.; Madhava, A. K. Chemosphere. 2021, 285, 131-480. DOI: https://doi/10.1016/j.chemosphere.2021.131480. DOI: https://doi.org/10.1016/j.chemosphere.2021.131480
Langmuir, I. J. Am. Che. Soc. J. 1918, 40, 1361-1403. DOI: https://doi/10.1021/ja02242a004. DOI: https://doi.org/10.1021/ja02242a004
Freundlich, H. M. F. Colloid and Capillary Chemistry, Methuen, London, UK, 1926.
Hossain, I.; Hossain, A.; Choudhury, I. A. J. Text. Inst. 2015, 107, 154-164. DOI: https://doi/10.1080/00405000.2015.1018669. DOI: https://doi.org/10.1080/00405000.2015.1018669
Savari, M.; Esfahani, S. H. Z.; Edalati, M.; Biria, D. Protein. Expr. Purif. 2015, 114, 128-135. DOI: https://doi/10.1016/j.pep.2015.06.006. DOI: https://doi.org/10.1016/j.pep.2015.06.006
Necib, Y.; Bahi, A.; Merouane, F.; Bouadi, H.; Boulahrouf, K. World. J. Pharm. Res. 2015, 4, 1720-1733.
Morris, G.; Huey, R.; Lindstrom, W.; Sanner, M.; Belew, R.; Goodsell, D.; Olson, A. J. Comput. Chem. 2009, 30, 2785–2791. DOI: https://doi.org/10.1002/jcc.21256.
Kausar, N.; Murtaza, S.; Nadeem Arshad, M.; Munir, R.; Saleem, R. S. Z.; Rafique, H. T. J. Mol. Struct. 2021, 1244, 130983. DOI: https://doi.org/10 .1016/j.molstruc.2021.130983. DOI: https://doi.org/10.1016/j.molstruc.2021.130983
Bensegueni, R.; Guergouri, M.; Bensouici, C.; Bencharif, M. J. Rep. Pharm. Sci. 2019, 8, 195-203. DOI: https://doi.org/10.4103/jrptps.JRPTPS_46_18.
Asghar, A.; Abdul Raman, A. A.; Wan Daud, W. M. A. A. Sci. World. J. 2014, 1-14. DOI: https://doi/10.1155/2014/869120. DOI: https://doi.org/10.1155/2014/869120
Montgomery, D. C.; Runger, G. C. Applied. Ed., John Wiley & Sons, Singapore, 2014.
Mohana, S.; Shrivastava, S.; Divecha, J.; Madamwar, D. Bioresour. Technol. 2008, 99, 562–569. DOI: https://doi/10.1016/j.biortech.2006.12.033. DOI: https://doi.org/10.1016/j.biortech.2006.12.033

Downloads
Published
Issue
Section
License
Copyright (c) 2024 Oussama Larabi, Afaf Amara-Rekkab, Mohamed Amine Didi, Amel Didi, Souad Feddane

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
Authors who publish with this journal agree to the following terms:
- Authors retain copyright and grant the journal right of first publication with the work simultaneously licensed under a Creative Commons Attribution License that allows others to share the work with an acknowledgement of the work's authorship and initial publication in this journal.
- Authors are able to enter into separate, additional contractual arrangements for the non-exclusive distribution of the journal's published version of the work (e.g., post it to an institutional repository or publish it in a book), with an acknowledgement of its initial publication in this journal.