Aliskiren Copper(II) Complex. Synthesis and Antioxidant Activity
DOI:
https://doi.org/10.29356/jmcs.v68i2.1981Keywords:
N-ligands, copper, antioxidants, EPR, superoxide dismutaseAbstract
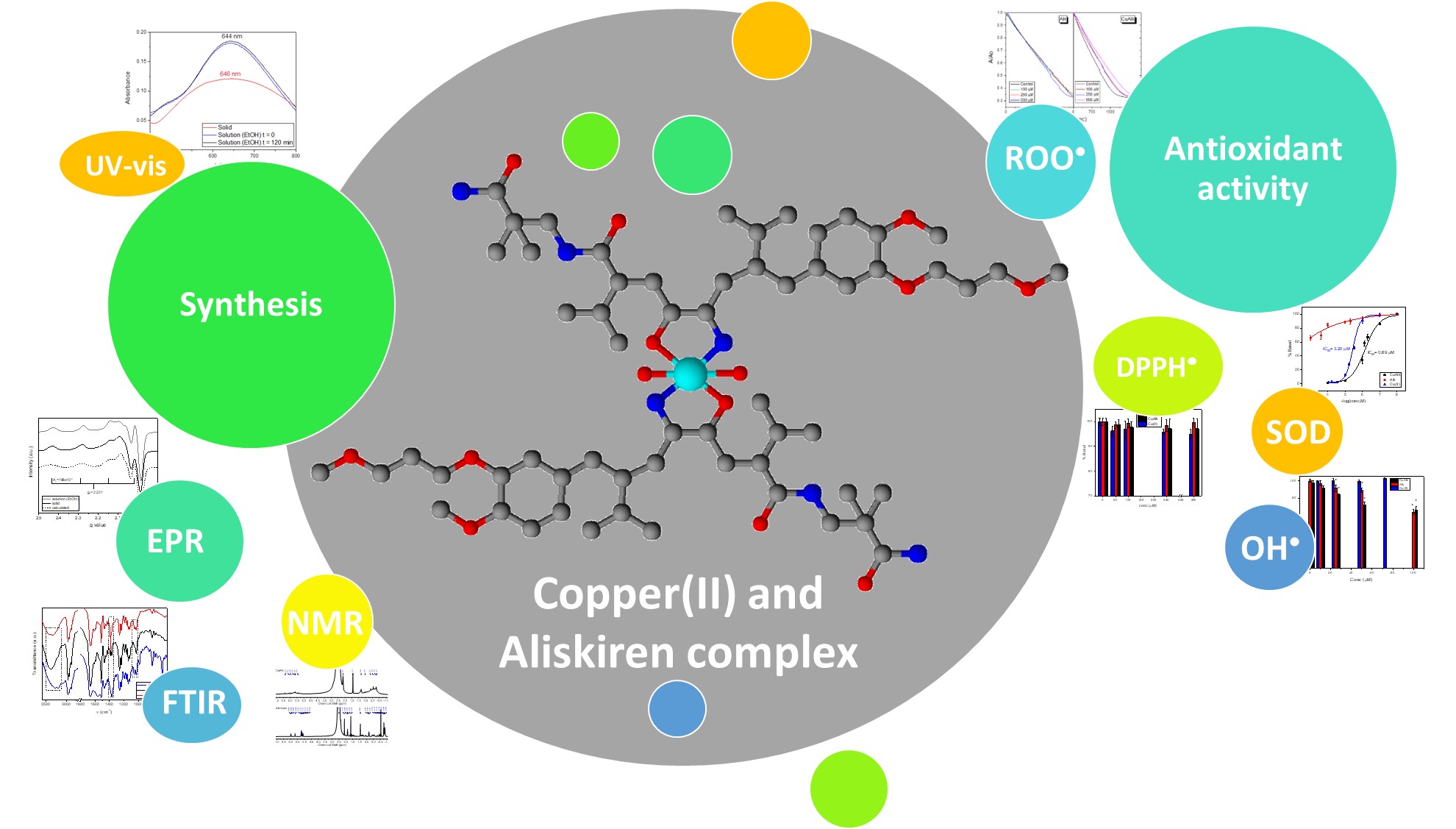
Abstract. Aliskiren (Alk) is a highly selective competitive inhibitor of renin used for the treatment of hypertension and related cardiovascular diseases. With the aim of improving its biological properties by the strategy of the induction of favorable conformational changes, we designed a metal-based drug. In this work we report the synthesis of a solid copper(II) complex with aliskiren, CuAlk, and its characterization in solution and solid-state. Moreover, and based on the association of hypertension with elevated levels of reactive oxygen species (ROS), the antioxidant properties of CuAlk were studied measuring the activities against 2,2-diphenyl-1-picrilhidrazil (DPPH·), hydroxyl (OH·) and peroxyl (ROO·) radicals, in addition to its superoxide dismutase (SOD) simil activity. Both the ligand and the complex were able to scavenge hydroxyl radicals, but upon complexation, the SOD mimetic activity of the ligand is enhanced.
Resumen. El Aliskiren (Alk) es un inhibidor por competencia altamente selectivo de la renina que se utiliza en el tratamiento de la hipertensión y enfermedades cardiovasculares relacionadas. Se diseñó un metalofármaco con la idea de mejorar las propiedades biológicas mediante la inducción de cambios conformacionales favorables. En este trabajo se reporta la síntesis de un complejo sólido de cobre(II) con aliskiren, CuAlk, junto con su caracterización en fase sólida y en solución. Además, de acuerdo con la relación que existe entre la hipertensión y los niveles elevados de especies reactivas de oxígeno (ROS), se estudian las propiedades antioxidantes del CuAlk frente a los radicales 2,2-difenil-1-picrilhidracilo (DPPH·), hidroxilo (OH·) y peroxilo (ROO·), además de la actividad superóxido dismutasa símil (SOD). Tanto el ligando, como el complejo fueron capaces de secuestrar radicales hidroxilos, pero, luego de la complejación, se mejoró la actividad SOD símil del ligando.
Downloads
References
Wood, J. M.; Maibaum, J.; Rahuel, J.; Grütter, M. G.; Cohen, N. C.; Rasetti, V.; Rüger, H.; Göschke, R.; Stutz, S.; Fuhrer, W.; Schilling, W.; Rigollier, P.; Yamaguchi, Y.; Cumin, F.; Baum, H. P.; Schnell, C. R.; Herold, P.; Mah, R.; Jensen, C.; O’Brien, E.; Stanton, A.; Bedigian, M. P. Biochem. Biophys. Res. Commun. 2003, 308, 698–705. DOI: https://doi.org/10.1016/s0006-291x(03)01451-7.
Cromer, J.; Peker, S. Pharm. Ther. 2008, 33, 92–96. DOI: https://doi.org/10.1177/1037969X0803300206
Alshahrani, S.; Tripathi, P.; Ashafaq, M.; Sultan, M. H.; Moni, S. S.; Tripathi, R.; Siddiqui, A. H.; Rashid, H.; Malhan, A. M. Toxin Rev. 2022, 41, 175–185. DOI: https://doi.org/10.1080/15569543.2020.1857772.
Alshahrani, S. Chem. Biol. Interact. 2020, 326, 109145. DOI: https://doi.org/10.1016/j.cbi.2020.109145.
Uriu-Adams, J.Y.; Keen, C.L. Mol Aspects Med. 2005, 26, 268-98. DOI: http://doi.org/10.1016/j.mam.2005.07.015. DOI: https://doi.org/10.1016/j.mam.2005.07.015
Bontchev, P.R.; Pantcheva, I.N. Trans. Met. Chem. 2002, 27, 1–21. DOI: https://doi.org/10.1023/A:1013466529495.
Islas, M.S.; Luengo, A.; Franca, C.A. Griera Merino, M.; Calleros, L.; Rodriguez-Puyol, M.; Lezama, L.; Ferrer, E.G.; Williams, P.A.M. J. Biol. Inorg. Chem. 2016, 21, 851–863. DOI: https://doi.org/10.1007/s00775-016-1384-5
Claudel, M.; Schwarte, J.V.; Fromm, K.M. Chemistry, 2020, 2, 849-899. DOI: https://doi.org/10.3390/chemistry2040056
Van Rijt, S.H., Sadler P.J. Drug Discov. Today 2009, 14, 1089-1097. DOI: https://doi.org/10.1016/j.drudis.2009.09.003
Baddiel, C. B.; Cavendish, C. D.; George, W. O. J. Mol. Struct. 1970, 5, 263–274. DOI: https://doi.org/10.1016/0022-2860(70)80029-1
Halliwell, B.; Gutteridge, J. M. C.; Aruoma, O. I. Anal. Biochem. 1987, 165, 215–219. DOI: https://doi.org/10.1016/0003-2697(87)90222-3.
Zhong, Z.; Ji, X.; Xing, R.; Liu, S.; Guo, Z. Bioorg. Med. Chem. 2007, 15, 3775–3782. DOI: https://doi.org/10.1016/j.bmc.2007.03.036.
Huang, W. Y.; Majumder, K.; Wu, J. Food Chem. 2010, 123, 635–641. DOI: https://doi.org/10.1016/j.foodchem.2010.04.083.
Islas, M. S.; Luengo, A.; Franca, C. A.; Merino, M. G.; Calleros, L.; Rodriguez-Puyol, M.; Lezama, L.; Ferrer, E. G.; Williams, P. A. M. J. Biol. Inorg. Chem. 2016, 21. DOI: https://doi.org/10.1007/s00775-016-1384-5.
Tabbì, G.; Giuffrida, A.; Bonomo, R. P. J. Inorg. Biochem. 2013, 128, 137–145. DOI: https://doi.org/10.1016/j.jinorgbio.2013.07.035.
Peisach, J.; Blumberg, W. E. Arch. Biochem. Biophys. 1974, 165, 691–708. DOI: https://doi.org/10.1016/0003-9861(74)90298-7.
Castinñeiras, A.; Balboa, S.; Carballo, R.; Niclós, J. Zeitschrift für Anorg. und Allg. Chemie 2002, 628, 2353–2359. DOI: https://doi.org/10.1002/1521-3749(200211)628:11%3C2353::AID-ZAAC2353%3E3.0.CO;2-5. DOI: https://doi.org/10.1002/1521-3749(200211)628:11<2353::AID-ZAAC2353>3.0.CO;2-5
Lever, A. B. P. Inorganic Electronic Spectroscopy, Second Edi.; Elsevier: Toronto, Canada, 1984.
Miyamoto, T.; Kamino, S. Odani, A.; Hiromura, M.; Enomoto, S. Chem. Lett. 2013, 42, 1099-1101. DOI: https://doi.org/10.1246/cl.130405.
Hureau, C.; Eury, H.; Guillot, R.; Bijani, C.; Sayen, S.; Solari, P.L.; Guillon, E.; Faller, P.; Dorlet, P. Chem. A Eur. J. 2011, 17, 10151–10160. DOI: http://doi.org/10.1002/chem.201100751. DOI: https://doi.org/10.1002/chem.201100751
Aydoǧmuş, Z.; Sari, F.; Ulu, S. T. J. Fluoresc. 2012, 22, 549–556. DOI: https://doi.org/10.1007/s10895-011-0988-y.
Kong, J.; Yu, S. Acta Biochim. Biophys. Sin. (Shanghai). 2007, 39, 549–559. DOI: https://doi.org/10.1111/j.1745-7270.2007.00320.x.
Nakamoto, K. Infrared and Raman Spectra of Inorganic and Coordination Compounds Part A; Wiley, 2009. DOI: https://doi.org/10.1002/9780470405840
Cacela, C.; Duarte, M. L.; Fausto, R. Spectrochim. Acta Part A Mol. Biomol. Spectrosc. 2000, 56, 1051–1064. DOI: https://doi.org/10.1016/S1386-1425(99)00203-6.
Matsoukas, M. T.; Zoumpoulakis, P.; Tselios, T. J. Chem. Inf. Model. 2011, 51, 2386–2397. DOI: https://doi.org/10.1021/ci200130m.
Islas, M. S.; Lezama, L.; Griera, M.; Cortes, M. A.; Rodriguez, M.; Ferrer, E. G.; Williams, P.A.M. J. Inorg. Biochem. 2013, 123, 23–33. DOI: https://doi.org/10.1016/j.jinorgbio.2013.02.005.
McCord, J. M.; Fridovich, I. J. Biol. Chem. 1969, 244, 6049–6055. DOI: https://doi.org/10.1016/S0021-9258(18)63504-5
Durot, S.; Policar, C.; Cisnetti, F.; Lambert, F.; Renault, J.; Pelosi, G.; Blain, G.; Korri-Youssoufi, H.; Mahy, J.-P. Eur. J. Inorg. Chem. 2005, 2005, 3513–3523. DOI: https://doi.org/10.1002/ejic.200400835.
Khalid, H.; Hanif, M.; Hashmi, M.; Mahmood, T.; Ayub, K.; Monim-ul-Mehboob, M. Mini-Reviews Med. Chem. 2013, 13, 1944–1956. DOI: https://doi.org/10.2174/13895575113136660092.
Szyrwiel, L.; Shimura, M.; Setner, B.; Szewczuk, Z.; Malec, K.; Malinka, W.; Brasun, J.; Pap, J. S. Int. J. Pept. Res. Ther. 2019, 25, 711–717. DOI: https://doi.org/10.1007/s10989-018-9717-6.

Downloads
Additional Files
Published
Issue
Section
License
Copyright (c) 2024 Nadir Jori, María Soledad Islas, Evelina Gloria Ferrer, Patricia Ana María Williams

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
Authors who publish with this journal agree to the following terms:
- Authors retain copyright and grant the journal right of first publication with the work simultaneously licensed under a Creative Commons Attribution License that allows others to share the work with an acknowledgement of the work's authorship and initial publication in this journal.
- Authors are able to enter into separate, additional contractual arrangements for the non-exclusive distribution of the journal's published version of the work (e.g., post it to an institutional repository or publish it in a book), with an acknowledgement of its initial publication in this journal.