Detection of the p53 Gene Mutation Using an Ultra-sensitive and Highly Selective Electrochemical DNA Biosensor
DOI:
https://doi.org/10.29356/jmcs.v67i1.1880Keywords:
p53 gene, electrochemical DNA biosensor, doxorubicin, cyclic voltammetryAbstract
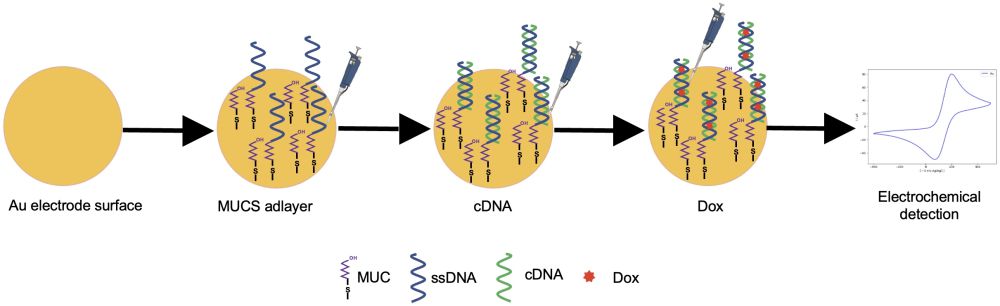
Abstract. The p53 gene— “the guardian of the genome”—is responsible for maintaining the integrity of the genome, along with cell cycle regulation, apoptosis, and cell differentiation. New analytical devices are needed to recognize the main alterations this gene could suffer, since it is one of the most frequent in human cancer. For this reason, we developed an electrochemical DNA biosensor with high sensitivity and specificity to monitor the 175p2 mutation of the p53 gene. We modified a screen-printed gold electrode (SPGE) by immobilizing a thiolated DNA probe sequence with 11-mercaptoundecanoic acid to detect its complementary sequence through the hybridization reaction. Doxorubicin (Dox) was used to increase the sensitivity of the biosensor, and the entire process was evaluated using the Cyclic Voltammetry (CV) technique. The measurement range of the developed device is from 1 fM to 100 nM of the p53 gene mutation with a limit of detection (LOD) of 2.2 fM. In the presence of Dox, the LOD increased up to 175 aM, becoming one of the highest efficiency devices in the field. The electrochemical DNA biosensor selectively detects the p53 suppressor gene mutation; it distinguishes between different non-complementary and complementary sequences. Our results indicate a high potential of our sensor for the p53 gene 175p2 mutation detection, which is convenient in the early diagnosis of diseases related to this gene.
Resumen. El gen p53—“guardián del genoma”—es responsable de mantener la integridad del genoma, así como de la regulación del ciclo celular, la apoptosis, y la diferenciación celular. Es necesario desarrollar nuevos dispositivos analíticos para reconocer las principales alteraciones que este gen podría sufrir, ya que es uno de los más frecuentes en el cáncer humano. En este sentido, se desarrolló un sensor electroquímico de ADN de alta sensibilidad y especificidad para identificar la mutación 175p2 del gen p53. Para ello, se formó una monocapa sobre un electrodo de oro que contenía secuencias sonda de ADN tiolado junto con ácido 11-mercaptoundecanoico, las cuales se emplearon para detectar la mutación del gen a través de la reacción de hibridación. Finalmente, se utilizó doxorrubicina (Dox) para aumentar la sensibilidad del biosensor; el proceso se evaluó mediante la técnica de Voltamperometría Cíclica (VC). El rango de medición del dispositivo desarrollado es de 1 fM a 100 nM de la mutación del gen p53 con un límite de detección (LOD) de 2.2 fM. En presencia de Dox, el LOD aumentó hasta 175 aM, convirtiéndose en uno de los dispositivos de mayor eficiencia en el campo. El biosensor electroquímico de ADN detecta selectivamente la mutación del gen supresor p53 y es capaz de distinguir entre diferentes secuencias complementarias y no complementarias. Nuestros resultados indican un alto potencial del biosensor para la detección de la mutación 175p2 del gen p53, lo cual es conveniente en el diagnóstico oportuno de enfermedades relacionadas con este gen.
Downloads
References
Wang, X.; Wang, X; Wang, X; Chen, F; Zhu, K.; Xu, Q.; Tang, M. Anal. Chim. Acta. 2013, 765, 63-69 DOI: https://doi.org/10.1016/j.aca.2012.12.037
Kang, J.; Li, Z.; Wang, G. Bioelectrochemistry. 2021, 137, 107647 DOI: https://doi.org/10.1016/j.bioelechem.2020.107647
Yang, L.; Tao, Y.; Yue, G.; Li, R.; Qiu, B.; Guo, L.; Lin, Z.; Yang, H.-H. Anal. Chem. 2016, 88, 5097-5103 DOI: https://doi.org/10.1021/acs.analchem.5b04521
Wang, Z.; Xia, J.; Song, D.; Zhang, F.; Yang, M.; Gui, R.; Xia, L.; Bi, S.; Xia, Y. Biosens. Bioelectron. 2016, 77, 157-163 DOI: https://doi.org/10.1016/j.bios.2015.09.011
Afsharan, H.; Khalilzadeh, B.; Tajalli, H.; Mollabashi, M.; Navaeipour, F.; Rashidi, M.-R. Electrochim. Acta. 2016, 188, 153-164 DOI: https://doi.org/10.1016/j.electacta.2015.11.133
Wang, W.; Gao, Y.; Wang, W.; Zhang, J.; Li, Q.; Wu, Z.-S. Anal. Chem. 2022, 94, 1029-1036 DOI: https://doi.org/10.1021/acs.analchem.1c03991
Fayazfar, H.; Afshar, A.; Dolati, M.; Dolati, A. Anal. Chim. Acta. 2014, 836, 34-44 DOI: https://doi.org/10.1016/j.aca.2014.05.029
Sohrabi, N.; Valizadeh, A.; Farkhani, S. M.; Akbarzadeh, A. Artif. Cells, Nanomed., Biotechnol. 2016, 44, 654-663 DOI: https://doi.org/10.3109/21691401.2014.976707
Deepa, Pundir, S.; Pundir, C. S. Anal. Biochem. 2020, 588, 113473 DOI: https://doi.org/10.1016/j.ab.2019.113473
Jayanthi, V. S. P. K. S. A.; Das, A. B.; Saxena, U. Biosens. Bioelectron. 2017, 91, 15-23 DOI: https://doi.org/10.1016/j.bios.2016.12.014
Naresh, V.; Lee, N. Sensors. 2021, 21, 1109 DOI: https://doi.org/10.3390/s2104110 DOI: https://doi.org/10.3390/s21041109
Quinchia, J.; Echeverri, D.; Cruz-Pacheco, A. F.; Maldonado, M. E.; Orozco, J. Micromachines. 2020, 11, 411 DOI: https://doi.org/10.3390/mi11040411
Kappo, D.; Shurpik, D.; Padnya, P.; Stoikov, I.; Rogov, A.; Evtugyn, G. Biosensors. 2021, 12, 329 DOI: https://doi.org/10.3390/bios12050329
Mousavisani, S. Z.; Raoof, J. B.; Ojani, R.; Valiollahi, R. Journal of Chemical Sciences. 2017, 129, 131-139 DOI: https://doi.org/10.1007/s12039-016-1198-6
Hamidi-Asl, E.; Raoof, J. B.; Hejazi, M. S.; Sharifi, S.; Golabi, S. M.; Palchetti, I.; Mascini, M. Electroanalysis. 2015, 27, 1378-1386 DOI: https://doi.org/10.1002/elan.201400660
Raoof, J. B.; Ojani, R.; Golabi, S. M.; Hamidi-Asl, E.; Hejazi, M. S. Sens. Actuators, B. 2011, 157, 195-201 DOI: https://doi.org/10.1016/j.snb.2011.03.049
Kerman, K.; Vestergaard, M.; Tamiya, E. Methods Mol. Biol. 2009, 504, 99-133 DOI: https://doi.org/10.1007/978-1-60327-569-9_7
Yang, F.; Teves, S. S.; Kemp, C. J.; Henikoff, S. Biochim. Biophys. Acta, Rev. Cancer. 2014, 1845, 84-89 DOI: https://doi.org/10.1016/j.bbcan.2013.12.002
Rasanang, N. S.; Nor, S. N. S.; Karman, S.; Zaman, W. S. W. K.; Harun, S. W.; Arof, H. 2022 IEEE 18th International Colloquium on Signal Processing & Applications (CSPA). 2022, 403–407 DOI: https://doi.org/10.1109/CSPA55076.2022.9781966
Sánchez-Obrero, G.; Humanes, I.; Madueño, R.; Sevilla, J. M.; Pineda, T.; Blázquez, M. Int. J. Mol. Sci. 2022, 23, 14132 DOI: https://doi.org/10.3390/ijms232214132
Bahner, N.; Reich, P.; Frense, D.; Menger, M.; Schieke, K.; Beckmann, D. Anal. Bioanal. Chem. 2018, 410, 1453-1462 DOI: https://doi.org/10.1007/s00216-017-0786-8
Ting, B. P.; Zhang, J.; Gao, Z.; Ying, J. Y. Biosens. Bioelectron. 2009, 25, 282–287 DOI: https://doi.org/10.1016/j.bios.2009.07.005
Van Nguyen, K.; Minteer, S. D. Chem. Commun. 2015, 51, 4782–4784 DOI: https://doi.org/10.1039/C4CC10250A
Lee, H.-E.; Kang, Y. O.; Choi, S.-H. Int. J. Electrochem. Sci. 2014, 9, 6793–6808 DOI: https://doi.org/10.1016/S1452-3981(23)10930-8
Grieshaber, D.; MacKenzie, R.; Voros, J.; Reimhult, E. Sensors. 2008, 8, 1400-1458 DOI: https://doi.org/10.3390/s80314000
Garcia-Melo, L. F.; Álvarez-González, I.; Madrigal-Bujaidar, E.; Madrigal-Santillán, E. O.; Morales-González, J. A.; Cruces, R. N. P.; Ramírez, J. A. C.; Matsumura, P. D.; Aguilar-Santamaría, M. de los Angeles; Batina, N. J. Electroanal. Chem. 2019, 840, 93-100 DOI: https://doi.org/10.1016/j.jelechem.2019.03.048
Elgrishi, N.; Rountree, K. J.; McCarthy, B. D.; Rountree, E. S.; Eisenhart, T. T.; Dempsey, J. L. J. Chem. Educ. 2018, 95, 197-206 DOI: https://doi.org/10.1021/acs.jchemed.7b00361
Rashid, J. I. A.; Yusof, N. A.; Abdullah, J.; Hashim, U.; Hajian, R. Materials Science and Engineering: C. 2014, 45, 270-276 DOI: https://doi.org/10.1016/j.msec.2014.09.010
Shen, H.; Mark, J. E.; Seliskar, C. J.; Mark, H. B.; Heineman, W. R. J. Solid State Electrochem. 1997, 1, 148-154. DOI: https://doi.org/10.1007/s100080050039
Hong, L.; Lu, M.; Dinel, M.-P.; Blain, P.; Peng, W.; Gu, H.; Masson, J.-F. Biosens. Bioelectron. 2018, 109, 230-236 DOI: https://doi.org/10.1016/j.bios.2018.03.032
Lee, L. Y. S.; Lennox, R. B. Phys. Chem. Chem. Phys. 2007, 8, 1013-1020 DOI: https://doi.org/10.1039/B613598F
Zhang, K.; Zhang, Y. Electroanalysis. 2010, 22, 673-679 DOI: https://doi.org/10.1002/elan.200900453
Attoye, B.; Baker, M. J.; Thomson, F.; Pou, C.; Corrigan, D. K. Biosensors. 2021, 11, 42 DOI: https://doi.org/10.3390/bios11020042
Evtugyn, G.; Porfireva, A.; Stepanova, V.; Budnikov, H. Electroanalysis. 2015, 27, 629–637 DOI: https://doi.org/10.1002/elan.201400564
Moghadam, F. H.; Taher, M. A.; Karimi-Maleh, H. Micromachines. 2021, 12, 808 DOI: https://doi.org/10.3390/mi12070808
Karimi-Maleh, H.; Alizadeh, M.; Orooji, Y.; Karimi, F.; Baghayeri, M.; Rouhi, J.; Tajik, S.; Beitollahi, H.; Agarwal, S.; Gupta, V. K.; Rajendran, S.; Rostamnia, S.; Fu, L.; Saberi-Movahed, F.; Malekmohammadi, S. Ind. Eng. Chem. Res. 2021, 60, 816-823 DOI: https://doi.org/10.1021/acs.iecr.0c04698
Ting, B. P.; Zhang, J.; Gao, Z.; Ying, J. Y. Biosens. Bioelectron. 2009, 25, 282-287 DOI: https://doi.org/10.1016/j.bios.2009.07.005
Aghili, Z.; Nasirizadeh, N.; Divsalar, A.; Shoeibi, S.; Yaghmaei, P. Artif. Cells, Nanomed., Biotechnol. 2017, 46, 32–40 DOI: https://doi.org/10.1080/21691401.2017.1411930
Taei, M.; Salavati, H.; Hasanpour, F.; Shafiei, A. IEEE Sens. J. 2016, 16, 24–31 DOI: https://doi.org/10.1109/JSEN.2015.2474262
Kulikova, T. N.; Porfireva, A. V.; Shamagsumova, R. V.; Evtugyn, G. A. Electroanalysis. 2018, 30, 2284–2292 DOI: https://doi.org/10.1002/elan.201800331
Hassani Moghadam, F.; Taher, M. A.; Karimi-Maleh, H. Micromachines. 2021, 12, 808 DOI: https://doi.org/10.3390/mi12070808
Ma, H.; Zhang, L.; Pan, Y.; Zhang, K.; Zhang, Y. Electroanalysis. 2008, 20, 1220–1226 DOI: https://doi.org/10.1002/elan.200704169
Jawad, B.; Poudel, L.; Podgornik, R.; Steinmetz, N. F.; Ching, W.-Y. Phys. Chem. Chem. Phys. 2019, 21, 3877–3893 DOI: https://doi.org/10.1039/C8CP06776G
Wang, Y.; Xia, L.; Wei, C.; Wang, H.; Wang, H.; Yuan, R.; Wei, S. Chem. Commun. 2019, 55, 13082–13084 DOI: https://doi.org/10.1039/C9CC06556C
Malanina, A. N.; Kuzin, Y. I.; Ivanov, A. N.; Ziyatdinova, G. K.; Shurpik, D. N.; Stoikov, I. I.; Evtugyn, G. A. Journal of Analytical Chemistry. 2022, 77, 185-194 DOI: https://doi.org/10.1134/S1061934822020095
Trotter, M.; Borst, N.; Thewes, R.; von Stetten, F. Biosens. Bioelectron. 2020, 154, 112069 DOI: https://doi.org/10.1016/j.bios.2020.112069
Helmerhorst, E.; Chandler, D. J.; Nussio, M.; Mamotte, C. D. Clin Biochem Rev. 2012, 33, 161-173
Han, S. H.; Kim, S. K.; Park, K.; Yi, S. Y.; Park, H. -J.; Lyu, H. -K.; Kim, M.; Chung, B. H. Anal. Chim. Acta. 2010, 665, 79-83 DOI: https://doi.org/10.1016/j.aca.2010.03.006
Liu, Y.; Chen, X.; Ma, Q. Biosens. Bioelectron. 2018, 117, 240-245 DOI: https://doi.org/10.1016/j.bios.2018.06.023
Wang, P.; Wu, H.; Dai, Z.; Zou, X. Chemical Communications. 2012, 48, 10754-10756 DOI: https://doi.org/10.1039/C2CC35615E
Yang, L.; Tao, Y.; Yue, G.; Li, R.; Qiu, B.; Guo, L.; Lin, Z.; Yang, H. -H. Anal. Chem. 2016, 88, 5097-5103 DOI: https://doi.org/10.1021/acs.analchem.5b04521
Ding, L.; Zhang, L.; Yang, H.; Liu, H.; Ge, S.; Yu, J. Sens. Actuators, B. 2018, 268, 210-216 DOI: https://doi.org/10.1016/j.snb.2018.04.126
Wang, P.; Wu, H.; Dai, Z.; Zou, X. Chemical Communications. 2012, 48, 10754-10756 DOI: https://doi.org/10.1039/C2CC35615E
Song, S.; Lee, J. U.; Kang, J.; Park, K. H.; Sim, S. J. Sens. Actuators, B. 2020. 322, 128584 DOI: https://doi.org/10.1016/j.snb.2020.128584
Zhou, W.; Ma, Y.; Yang, H.; Ding, Y.; Luo, X. Int. J. Nanomed. 2011, 6, 381-386 DOI: https://doi.org/10.2147/IJN.S13249
Wang, J.; Rivas, G.; Cai, X.; Chicharro, M.; Parrado, C.; Dontha, N.; Begleiter, A.; Mowat, M.; Palecek, E.; Nielsen, P. E. Anal. Chim. Acta. 1997, 344, 111-118 DOI: https://doi.org/10.1016/S0003-2670(97)00039-1
Hou, L.; Huang, Y.; Hou, W.; Yan, Y.; Liu, J.; Xia, N. Int. J. Biol. Macromol. 2020, 158, 580-586 DOI: https://doi.org/10.1016/j.ijbiomac.2020.04.271
Wang, J.; Zhu, X.; Tu, Q.; Guo, Q.; Zarui, C. S.; Momand, J.; Sun, X. Z.; Zhou, F. Anal. Chem. 2008, 80, 769-774 DOI: https://doi.org/10.1021/ac0714112
Qiu, S.; Li, X.; Xiong, W.; Xie, L.; Guo, L.; Lin, Z.; Qiu, B.; Chen, G. Biosens. Bioelectron. 2013, 41, 403-408 DOI: https://doi.org/10.1016/j.bios.2012.08.065
Du, D.; Wang, L.; Shao, Y.; Wang, J.; Engelhard, M. H.; Lin, Y. Anal. Chem. 2011, 83, 746-752 DOI: https://doi.org/10.1021/ac101715s
Amor-Gutiérrez, O.; Costa-Rama, E.; Arce-Varas, N.; Martínez-Rodríguez, C.; Novelli, A.; Fernández-Sánchez, M. T.; Costa-García, A. Anal. Chim. Acta. 2020, 1093, 28-34 DOI: https://doi.org/10.1016/j.aca.2019.09.042
Xie, Y.; Chen, A.; Du, D.; Lin, Y. Anal. Chim. Acta. 2011, 699, 44-48 DOI: https://doi.org/10.1016/j.aca.2011.05.010
Hamidi-Asl, E.; Raoof, J. B.; Ojani, R.; Hejazi, M. S. Electroanalysis. 2013, 25, 2075-2083 DOI: https://doi.org/10.1002/elan.201300155
Wang, X.; Zhang, X.; He, P.; Fang, Y. Biosens. Bioelectron. 2011, 26, 3608-3613 DOI: https://doi.org/10.1016/j.bios.2011.02.012
Zhang, D. Y.; Chen, S. X.; Yin, P. Nat. Chem. 2012, 4, 208-214 DOI: https://doi.org/10.1038/nchem.1246
Ge, D.; Wang, X.; Williams, K.; Levicky, R. Langmuir. 2012, 28, 8446-8455 DOI: https://doi.org/10.1021/la301165a
Castañeda, M. T.; Merkoçi, A.; Pumera, M.; Alegret, S. Biosens. Bioelectron. 2007, 22, 1961-1967 DOI: https://doi.org/10.1016/j.bios.2006.08.031
Long, Y.-T.; Li, C.-Z.; Sutherland, T. C.; Kraatz, H.-B.; Lee, J. S. Anal. Chem. 2004, 76, 4059-4065 DOI: https://doi.org/10.1021/ac049482d
Azimzadeh, M.; Nasirizadeh, N.; Rahaie, M.; Naderi-Manesh, H. RSC Adv. 2017, 7, 55709–55719 DOI: https://doi.org/10.1039/C7RA09767K

Downloads
Published
Issue
Section
License
Copyright (c) 2023 Luis Fernando Garcia-Melo, Norma Andrea Chagoya Pio, Miguel Morales-Rodríguez, Eduardo Madrigal-Bujaidar, Eduardo O. Madrigal-Santillán, Isela Álvarez-González, Rosa N. Pineda Cruces, Nikola Batina

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
Authors who publish with this journal agree to the following terms:
- Authors retain copyright and grant the journal right of first publication with the work simultaneously licensed under a Creative Commons Attribution License that allows others to share the work with an acknowledgement of the work's authorship and initial publication in this journal.
- Authors are able to enter into separate, additional contractual arrangements for the non-exclusive distribution of the journal's published version of the work (e.g., post it to an institutional repository or publish it in a book), with an acknowledgement of its initial publication in this journal.